A drop of solution (volume 0.05 mL) contains 3.0 x10-6 mole of H+. If the rate constant of disappearance of H+ is 1.0x107 mol litre sec?. How long would it take for H+ in drop to disappear?
1. 6x10-8 sec
2. 6x10-7 sec
3. 6x10-9 sec
4. 6x10-10 sec
विलयन (आयतन 0.05 mL) की एक बूंद में H+ के 3.0 x10-6 मोल होते हैं। यदि H+ के विलुप्त होने की दर स्थिरांक 1.0x107 मोल लीटर सेकंड है? बूंद में H+ के लिए विलुप्त होने में कितना समय लगेगा?
(1) 6x10-8 sec
(2) 6x10-7 sec
(3) 6x10-9 sec
(4) 6x10-10 sec
For a reaction A Product, rate law is . The concentration of A left after time t when is:
1.
2.
3.
4.
Aउत्पाद, अभिक्रिया के लिए, दर नियम है। जब , A की सांद्रता समय t के बाद शेष है:
(1)
(2)
(3)
(4)
Mechanism of a hypothetical reaction
is given below
(i)
(ii)
(iii)
The overall order of the reaction will be
(a) 1
(b) 2
(c) 0
(d) 1.5
एक काल्पनिक अभिक्रिया की क्रियाविधि
नीचे दिया गया है
(i)
(ii)
(iii)
अभिक्रिया की समग्र कोटि होगी
(1) 1
(2) 2
(3) 0
(4) 1.5
The half-life period of a first order chemical reaction is 6.93 minutes. The time required for the completion of 99% of the chemical reaction will be (log 2 = 0.301):
1. 23.03 minutes
2. 46.06 minutes
3. 460.6 minutes
4. 230.3 minutes
प्रथमकोटि रासायनिक अभिक्रिया का अर्ध आयु काल 6.93 मिनट है। 99% रासायनिक अभिक्रिया के पूर्ण होने के लिए आवश्यक समय होगा (log 2 = 0.301):
(1) 23.03 मिनट
(2) 46.06 मिनट
(3) 460.6 मिनट
(4) 230.3 मिनट
The time for half-life of a first order reaction is 1 hr. What is the time taken for 87.5% completion of the reaction?
1. 1 hour
2. 2 hour
3. 3 hour
4. 4 hour
प्रथम कोटि की अभिक्रिया का अर्ध आयु काल 1 घंटा है। 87.5% अभिक्रिया पूर्ण होने में कितना समय लगता है?
(1) 1 घंटा
(2) 2 घंटा
(3) 3 घंटा
(4) 4 घंटा
A reaction A2 + B2 2AB occurs by the following mechanism;
A2 A + A .....(slow)
A + B2 AB + B .....(fast)
A + B AB .....(fast)
Its order would be:
1. 3/2
2. 1
3. zero
4. 2
एक अभिक्रिया A2+ B2 2AB निम्नलिखित क्रियाविधि द्वारा होती है;
A2 A + A ..... (धीमा)
A + B2 AB + B ..... (तेज)
A + B AB..... (तेज)
इसकी कोटि होगी:
(1) 3/2
(2) 1
(3) शून्य
(4) 2
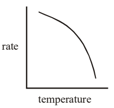
Which of the following correctly represents the variation of the rate of the reaction with temperature ?
(A) 
(B)
(C) 
(D)
निम्नलिखित में से कौन सा तापमान के साथ अभिक्रिया की दर की परिवर्तन को सही ढंग से दर्शाता है?
(1)
(2)
(3) 
(4)
Assertion : Liquid bromine reacts slowly as compared to bromine vapour.
Reason : In liquid bromine, the bromine molecules are held together by a force which is much weaker than the force existing between the two molecules of bromine in the vapour phase.
अभिकथन: ब्रोमीन वाष्प की तुलना में द्रव ब्रोमीन धीरे-धीरे अभिक्रिया करती है।
कारण: द्रव ब्रोमीन में, ब्रोमीन के अणुओं को एक बल द्वारा एक साथ धारण किए जाते हैं जो वाष्प प्रावस्था में ब्रोमीन के दो अणुओं के बीच उपस्थित बल से बहुत दुर्बल होता है।
- If both the assertion and the reason are true and the reason is a correct explanation of the assertion
- If both the assertion and reason are true but the reason is not a correct explanation of the assertion
- If the assertion is true but the reason is false
- If both the assertion and reason are false
Rate constant of reaction can be expressed by Arrhenius equation as,
In this equation, represents:
1. the energy above which all the colliding molecules will react
2. the energy below which colliding molecules will not react
3. the total energy of the reacting molecules at a temperature, T
4. the fraction of molecules with energy greater than the activation energy of the reaction
आरेनियस समीकरण द्वारा अभिक्रिया की दर स्थिरांक इसप्रकार व्यक्त की जा सकती है,
इस समीकरण में, निरूपित करता है:
(1) वह ऊर्जा जिसके ऊपर सभी संघट्ट अणु अभिक्रिया करेंगे
(2) वह ऊर्जा जिसके नीचे सभी संघट्ट अणु अभिक्रिया नहीं करेंगे
(3) एक तापमान,T पर अभिक्रियाशील अणुओं की कुल ऊर्जा
(4) अभिक्रिया की सक्रियण ऊर्जा से अधिक ऊर्जा वाले अणुओं का अंश
In a reaction, the rate expression is, rate = K[A][B]2/3[C]0 , the order of reaction is:
1. 1
2. 2
3. 5/3
4. zero
एक अभिक्रिया में, दर व्यंजक, दर = K[A][B]2/3[C]0 है, अभिक्रिया की कोटि है:
1. 1
2. 2
3. 5/3
4. शून्य