If 'I' is the intensity of absorbed light and 'c' is the concentration of AB for the photochemical process AB + hv→ AB *, the rate of formation of AB * is directly proportional to:
1. c
2. I
3. I2
4. cI
यदि 'I' अवशोषित प्रकाश की तीव्रता है और 'c', प्रकाशरासायनिक प्रक्रम AB + hv → AB* के लिए AB की सांद्रता है, AB* के बनने की दर सीधे समानुपाती है:
(1) c
(2) I
(3) I2
(4) cI
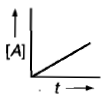
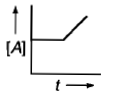
Which curve represents zero order reaction?
1.
2.
3.
4.
कौन सा वक्र शून्य कोटि अभिक्रिया को निरूपित करता है?
(1)
(2)
(3)
(4)
Find out the percentage of the reactant molecules crossing over the energy bariier at 325 K, given that
1. 80.62 %
2. 85.23 %
3. 89.27 &
4. None of the above
325 K पर ऊर्जा अवरोध को पार करने वाले अभिकारक अणुओं का प्रतिशत ज्ञात कीजिए, दिया गया है कि
1. 80.62 %
2. 85.23 %
3. 89.27 %
4. उपरोक्त में से कोई नहीं
Rate constant for a chemical reaction takes place at 500 K, is expressed as K = A e-1000. The activation energy of the reaction is
1. 100 cal/mol
2. 1000 kcal/mol
3. 104 kcal/mol
4. 106 kcal/mol
रासायनिक अभिक्रिया के लिए दर स्थिरांक 500 K पर, जिसे K = A e-1000 के रूप में व्यक्त किया जाता है। अभिक्रिया की सक्रियता ऊर्जा है:
1. 100 cal/mol
2. 1000 kcal/mol
3. 104 kcal/mol
4. 106 kcal/mol
The rate constant for a reaction of zero orde in A is 0.0030 mol L-1 s-1.How long will it take for the initial concentration of A to fall from 0.10 M to 0.075 M?
1.8.3 sec
2. 0.83 sec
3. 83 sec
4.10.3 sec
A में शून्य कोटि अभिक्रिया के लिए दर स्थिरांक 0.0030 mol-1 s-1 L है 0.10 M से 0.075 M तक A की प्रारंभिक सांद्रता में कितना समय लगेगा?
1. 8.3 sec
2. 0.83 sec
3. 83 sec
4. 10.3 sec
A hypothetical reaction, A2 +B2 2AB mechanism as given below;
A2 A+ A ............(Fast)
A+B2 → AB + B ............(Slow)
A+ B → AB ............(Fast)
The order of the overall reaction is:
1. 2
2. 1
3. 1.5
4. zero
एक काल्पनिक अभिक्रिया, A2 +B2 2AB क्रियाविधि नीचे दी गई है:
A2 A + A ............ (तेज)
A+B2 → AB + B ............(धीमा )
A+ B → AB ............ (तेज)
समग्र अभिक्रिया की कोटि है:
1. 2
2. 1
3. 1.5
4. शून्य
A first order reaction was started with a decimolar solution of the reactant. After 8 minutes and 20 seconds, its concentration was found to be M/100. Determine the rate constant of the reaction.
(A)
(B)
(C)
(D)
प्रथम कोटि अभिक्रिया अभिकारक के डेसीमोलर विलयन के साथ प्रारंभ हुई थी। 8 min और 20 sec के बाद, इसकी सांद्रता M/100 पाई गई। अभिक्रिया का दर स्थिरांक निर्धारित कीजिए।
(1)
(2)
(3)
(4)
The half life time for the decomposition of a substance dissolved in is 2.5 hour at C. How much of the substance will be left after 10 hours, if the initial weight of the substance is 160 gm ?
1. 20 gm
2. 30 gm
3. 40 gm
4. 10 gm
C पर में घुले हुए किसी पदार्थ के विघटन के लिए अर्ध आयु काल 2.5 hour है। 10 hour के बाद पदार्थ का कितना भाग बचेगा, यदि पदार्थ का प्रारंभिक भार 160 gm है?
(1) 20 gm
(2) 30 gm
(3) 40 gm
(4) 10 gm
In Arrhenius equation K = Ae-Ea/RT, the quantity e-E/kT is referred as:
1. Boltzmann factor
2. frequency factor
3. activation factor
4. none of these
आरेनियस समीकरण K = Ae-Ea/RT में, परिमाण e-E/kT किसके रूप में संदर्भित किया जाता है:
1. बोल्ट्ज़मान गुणक
2. आवृत्ति गुणक
3. सक्रियण गुणक
4. इनमें से कोई नहीं
The rate of a chemical reaction doubles for every 10°C rise of temperature. If the temperature is raised by 50°C, the rate of the reaction increases by about :
1. 10 times
2. 24 times
3. 32 times
4. 64 times
The rate of a chemical reaction doubles for every 10°C rise of temperature. If the temperature is raised by 50°C, the rate of the reaction increases by about :
तापमान के प्रत्येक 10°C वृद्धि की पर एक रासायनिक अभिक्रिया की दर दोगुनी हो जाती है। यदि तापमान 50°C से बढ़ाया जाता है, तो अभिक्रिया की दर लगभग बढ़ जाती है:-
1. 10 गुना
2. 24 गुना
3. 32 गुना
4. 64 गुना