From the fact that the length of the side of a unit cell of lithium is 351 pm. Calculate its
atomic radius. Lithium forms body-centered cubic crystals.
(1) 152.69 pm
(2) 62.71 pm
(3) 151.98 pm
(4) 54.61 pm
इस तथ्य से कि लीथियम की एक एकक कोष्ठिका के भुजा की लंबाई 351 pm है। इसकी परमाणु त्रिज्या की गणना करें। लीथियम अंत:केंद्रित घनीय क्रिस्टल निर्मित करता है।
(1) 152.69pm
(2) 62.71pm
(3) 151.98pm
(4) 54.61pm
Assertion : An important feature of Fluorite structures is that cations being large in size occupy FCC
lattice points whereas anions occupy all the tetrahedral voids giving the formula unit (A: cation B: anion).
Reason : There are 6 cations and 12 anions per FCC unit cell of the Fluorite structure.
अभिकथन: फ्लुओराइड संरचनाओं की एक महत्वपूर्ण विशेषता यह है कि धनायन आकार में बड़े होने के कारण FCC जालक बिंदुओं पर कब्जा करते हैं, जबकि ऋणायन इकाई सूत्र (A: धनायन B: ऋणायन) देने वाले सभी चतुष्फलकीय रिक्तियों पर कब्जा करते हैं।
कारण: फ्लुओराइड संरचना के प्रति FCC एकक कोष्ठिका में 6 धनायन और 12 ऋणायन हैं।
- If both the assertion and the reason are true and the reason is a correct explanation of the assertion
- If both the assertion and reason are true but the reason is not a correct explanation of the assertion
- If the assertion is true but the reason is false
- If both the assertion and reason are false
Silver crystallizes in a face centred cubic system, 0.408 nm along each edge. The density of silver is 10.6 and the atomic mass is 107.9 g/mol. Calculate Avogadro's number.
(1) atom/mol
(2) atom/mol
(3) atom/mol
(4) atom/mol
सिल्वर एक फलक केंद्रित घनीय समुदाय, 0.408nm में प्रत्येक कोर के साथ क्रिस्टलीकृत होता है। सिल्वर का घनत्व 10.6 है और परमाणु द्रव्यमान 107.9 g/mol है। आवोगाद्रो संख्या की गणना कीजिए।
(1) atom/mol
(2) atom/mol
(3) atom/mol
(4) atom/mol
The n of a cubic unit cell is 4. The type of cell as-
(1) Body centred
(2) Face centred
(3) Primitive
(4) None of these
घनीय एकक कोष्ठिका का n 4 है सेल का प्रकार है-
(1) अंत: केंद्रित
(2) फलक केंद्रित
(3) आद्य
(4) इनमें से कोई नहीं
A rhombohedral unit cell is shown. What is its volume ?
Side length = a Å.
(1)
(2)
(3)
(4)
एक त्रिसमनताक्ष एकक कोष्ठिका दिखाई गयी है। इसका आयतन क्या है?
भुजा की लंबाई = a Å.
(1)
(2)
(3)
(4)
In the unit cell of an fcc system, the number of octahedral and tetrahedral holes are
(1) 4,4
(2) 4, 8
(3) 1, 8
(4) 4, 1
एक fcc समुदाय की एकक कोष्ठिका में अष्टफलकीय और चतुष्फलकीय छिद्र की संख्या होती है
(1) 4,4
(2) 4, 8
(3) 1, 8
(4) 4, 1
8 : 8 co-ordination of CsCl is found to change into 6 : 6
co-ordination on:
(1) applying pressure
(2) increasing temperature
(3) both (a) and (b)
(4) none of these
CsCl का 8: 8 उपसहसंयोजन 6: 6 उपसहसंयोजन में परिवर्तित होता है:
(1) दाब डालने पर
(2) तापमान बढ़ने पर
(3) दोनों (1) और (2)
(4) इनमें से कोई नहीं
Which is covalent solid?
1. Silicate
2. Diamond
3. Graphite
4. All of these
कौन सा सहसंयोजक ठोस है?
(1) Fe2O3
(2) हीरा
(3) ग्रेफाइट
(4) ये सभी
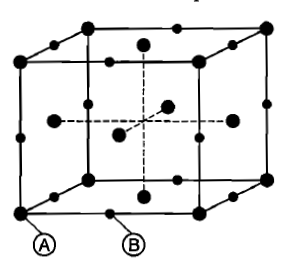
For a solid with the following structure, the co-ordination number of the point B is:
1. 3
2. 4
3. 5
4. 6
निम्नलिखित संरचना के साथ एक ठोस के लिए, बिंदु B की उपसहसंयोजन संख्या है:
(1) 3
(2) 4
(3) 5
(4) 6
A solid has a structure in which W atoms are located at the corners of a cubic lattice. Oxygen atom at the centre of the edges and Na atom at centre of the cube. The formula of the compound is
1. NaWO2
2. NaWO3
3. Na2WO3
4. NaWO4
एक ठोस में एक संरचना होती है जिसमें W परमाणु एक घनीय जालक के कोनों पर स्थित होते हैं। कोरों के केंद्र में ऑक्सीजन परमाणु और घन के केंद्र में Na परमाणु पर है। यौगिक का सूत्र है
1. NaWO2
2. NaWO3
3. Na2WO3
4. NaWO4





