P-V diagram of a diatomic gas is a straight line passing through origin. The molar heat capacity of the gas in the process will be -
1. 4 R
2. 2.5 R
3. 3 R
4.
किसी द्विपरमाणुक गैस के लिए P-V आरेख मूलबिंदु से गुजरने वाली एक सरल रेखा है। इस प्रक्रम में गैस की मोलर ऊष्मा धारिता होगी -
(1) 4R
(2) 2.5R
(3) 3R
(4)
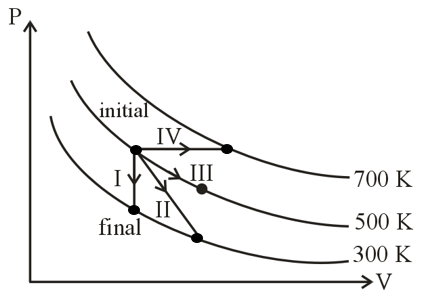
Match the following
Column-I Column-II
P. Process I a. Adiabatic
Q. Process II b. Isobaric
R. Process III c. Isochoric
S. Process IV d. Isothermal

निम्नलिखित का मिलान कीजिए
स्तम्भ-I स्तंभ-II
P. प्रक्रम I रुद्धोष्म
Q. प्रक्रम II समदाबीय
R. प्रक्रम III समआयतनिक
S. प्रक्रम IV समतापीय
In the following P-V diagram two adiabatics cut two isothermals at temperatures T1 and T2 (fig.). The value of will be
(1)
(2)
(3)
(4) VbVc
निम्नलिखित P-V आरेख में दो रुद्धोष्म वक्र तापमान T1 और T2 (आकृति) पर दो समतापी वक्रों को काटते हैं। का मान होगा :
(1)
(2)
(3)
(4) VbVc
In pressure-volume diagram given below, the isochoric, isothermal, and isobaric parts respectively are -
(1) BA, AD, DC
(2) DC, CB, DA
(3) AB, BC, CD
(4) CD, DA, AB
नीचे दिए गए दाब-आयतन आरेख में क्रमशः समआयतनिक, समतापीय और समदाबी भाग हैं: -
(1) BA, AD, DC
(2) DC, CB, DA
(3) AB, BC, CD
(4) CD, DA, AB
Four curves A, B, C and D are drawn in the adjoining figure for a given amount of gas. The curves which represent adiabatic and isothermal changes are -
(1) C and D respectively
(2) D and C respectively
(3) A and B respectively
(4) B and A respectively
गैस की दी गई मात्रा के लिए चार वक्र A, B, C और D संलग्न आकृति में खींचे गए है। वक्र जो रूद्धोष्म और समतापी परिवर्तनों को प्रदर्शित करते हैं -
(1) C और D क्रमश:
(2) D और C क्रमश:
(3) A और B क्रमश:
(4) B और A क्रमश:
The specific heat at constant pressure and at constant volume for an ideal gas are and and its adiabatic and isothermal elasticities are and respectively. The ratio of to is
(a)
(b)
(c)
(d)
एक आदर्श गैस के लिए नियत दाब और नियत आयतन पर विशिष्ट उष्मायें क्रमश: और है और इसकी रूद्धोष्म और समतापीय प्रत्यास्थताएँ क्रमशः और हैं। से का अनुपात ज्ञात कीजिए:
(a)
(b)
(c)
(d)
The temperature-entropy diagram of a reversible engine cycle is given in the figure. Its efficiency is
| 1. | 1/3 | 2. | 2/3 |
| 3. | 1/2 |
4. | 1/4 |
उत्क्रमणीय इंजन चक्र का तापमान-एन्ट्रॉपी आरेख आकृति में दिया गया है। इसकी दक्षता है :
| 1. | 1/3 | 2. | 2/3 |
| 3. | 1/2 |
4. | 1/4 |
When a system is taken from state i to a state f along path iaf, Q = 50 J and W = 20 J.
If W = –13 J for the curved return path fi, Q for this path is -
| 1. | 33 J | 2. | 23 J |
| 3. | – 7 J | 4. | – 43 J |
जब एक निकाय को पथ iaf के अनुदिश अवस्था i से अवस्था f तक ले जाया जाता है, Q = 50 J और W = 20 J
यदि पुनरागमन वक्राकार पथ fi के लिए W = –13 J, इस पथ के लिए Q है:
| 1. | 33 J | 2. | 23 J |
| 3. | – 7 J |
4. | – 43 J |
A cyclic process ABCA is shown in the V-T diagram. Process on the P-V diagram is -
| 1. |  |
2. |  |
| 3. |  |
4. |  |
एक चक्रीय प्रक्रम ABCA को V-T आरेख में दिखाया गया है। संगत P-V आरेख है -
| 1. |  |
2. |  |
| 3. |  |
4. |  |
An ideal monoatomic gas expands in such a manner that its pressure and volume can be related by equation . During this process, the gas is
(1) Heated
(2) Cooled
(3) Neither heated nor cooled
(4) First heated and then cooled
एक आदर्श एकपरमाणुक गैस इस प्रकार से प्रसारित होती है कि इसके दाब और आयतन को समीकरण द्वारा संबंधित किया जा सकता है। इस प्रक्रम के दौरान गैस:
(1) गर्म होती है
(2) ठंडी होती है
(3) न तो गर्म और न ही ठंडी होती है
(4) पहले गर्म और फिर ठंडी होती है













